LAPAROSCOPIC RETROPERITONEAL LYMPHADENECTOMY AFTER CHEMOTHERAPY FOR STAGE IIB TESTICULAR TUMORS
MIRANDOLINO B. MARIANO, MARCOS V. TEFILLI
Section of Urology, Hospital Mãe de Deus, Porto Alegre, RS, Brazil
ABSTRACT
Purpose:
We report our initial experience with laparoscopic retroperitoneal lymph
node dissection (LRLND) after chemotherapy in patients with clinical stage
IIb testicular carcinoma.
Material and Methods: Between March 1991
and April 2001, 5 patients underwent LRLND following initial chemotherapy
for stage IIb (1.5 to 5 cm) solitary or unilateral lymph node metastases.
Results: LRLND could be completed in all
cases. One patient had an inferior vena cava injury that was repaired
laparoscopically. This patient had a severe hypotension at the end of
the procedure and was reviewed laparoscopically, but no abnormalities
were found. Operative time was 150 to 380 minutes and blood loss was minimal.
The number of lymph nodes excised ranged from 12 to 36 (mean = 18.6).
Histological examination revealed necrosis in 4 cases and mature teratoma
in 1 case. Antegrade ejaculation was preserved in all patients. Mean hospital
stay was 3 days. There were no recurrences with a mean follow up of 12
months.
Conclusions: LRLND is a technically advanced
procedure that was both feasible and effective for exploration of stage
IIb testicular cancer after chemotherapy.
Key words:
testis; testicular neoplasms; chemotherapy; lymph node excision; laparoscopy
Braz J Urol, 27: 527-534, 2001
INTRODUÇÃO
A
linfadenectomia retroperitoneal é um procedimento cirúrgico
de grande porte e que confere considerável morbidade adicional
a pacientes portadores de neoplasias testiculares avançadas e já
debilitados pelos efeitos da quimioterapia (Qt). Neste contexto, o raciocínio
teórico estabelecido é que esta população
de pacientes pós-Qt poderia ser submetida a linfadenectomia retroperitoneal
laparoscópica (LRPL), reduzindo-se a morbidade e sem causar prejuízo
em termos de controle da doença, semelhante ao que ocorre com as
LRPL para tumores não-seminomatosos estágio-I (1-9). Na
literatura de língua inglesa revisada, dois trabalhos abordam a
questão da LRPL pós-Qt em tumores testiculares. Em 1996,
Rassweiler et al., após análise de 9 casos, concluem que
o procedimento não seria recomendado neste cenário clínico
(9). Em uma segunda publicação de 1999, Janetschek et al.demonstraram,
em 24 pacientes, que a LRPL pós-Qt é exeqüível,
reduzindo a morbidade e não comprometendo, a médio prazo,
o controle oncológico (4). Entretanto, foram incluídos no
protocolo apenas pacientes com massas retroperitoneais de até 5
cm antes da Qt, e não superiores a 3.5 cm pós-Qt (4).
Os autores apresentam sua experiência
inicial com LRPL pós-Qt, discutindo indicações, aspectos
técnicos e morbidade em pacientes com neoplasias testiculares estágio
clínico IIb.
MATERIAL E MÉTODOS
No
período de março de 1991 a abril de 2001, 31 pacientes com
idade entre 21 e 67 anos foram submetidos a LRPL e/ou exploração
laparoscópica de massas retroperitoneais, com as mais diversas
finalidades, por um dos 2 autores. Os pacientes eram provenientes de clínica
privada ou tiveram as cirurgias realizadas a pedido de colegas. Todos
os pacientes tinham prontuário disponível ou poderiam ser
facilmente contatados se necessário.
Da análise retrospectiva desta população,
foram identificados 5 casos de LRPL pós-Qt para tratamento de neoplasias
testiculares avançadas, os quais transformaram-se, então,
no alvo deste estudo. A média de idade da população
estudada foi de 32 anos (21 a 43 anos). O exame inicial da peça
de orquiectomia revelou seminoma puro em um paciente e neoplasias mistas
com e sem elementos de teratoma, respectivamente, em 3 e 1 caso. Todos
os tumores analisados foram neoplasias testiculares direitas. O estadiamento
foi realizado de acordo com as orientações internacionais
vigentes, empregando-se tomografia computadorizada (TC) de tórax
e abdômen e marcadores tumorais (alfa-feto proteína e fração
beta da gonadotrofina coriônica). Neste estudo, foram considerados
tumores estágio clínico IIb aqueles com linfonodos retroperitoneais
entre 1.5 e 5 cm de diâmetro, ou com mais de 6 linfonodos de até
1 cm (10). Todos os pacientes foram submetidos a Qt padrão, tendo
como base do esquema adotado o cisplatinum em 3 ou 4 ciclos, a critério
do oncologista envolvido no caso. Ao exame tomográfico, as massas
retroperitoneais pré-Qt variaram de 3 a 9 cm e o tamanho das mesmas
pós-Qt oscilou entre 1.5 e 5 cm. O estadiamento pós-Qt revelou
tumores testiculares estágio clínico IIb em todos os casos.
Metástase única foi encontrada em 4 pacientes e unilateral
múltipla com duas lesões em um. Nenhum dos pacientes submetidos
a LRPL tinha metástases bilaterais, doença metastática
fora do retroperitônio ou marcadores tumorais positivos no momento
da intervenção cirúrgica. A Table-1 apresenta alguns
dados referentes à população que foi alvo deste estudo.
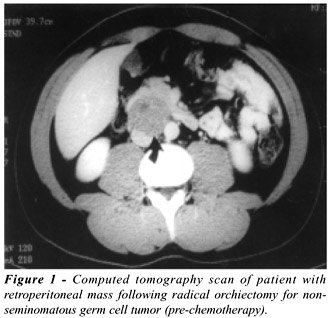
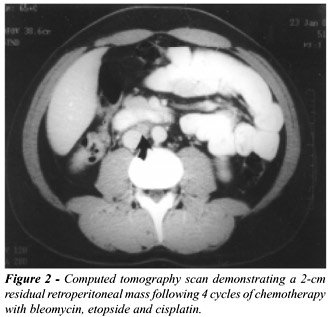
As Figures-1 e 2 ilustram um dos casos da presente série com achados
tomográficos pré e pós-Qt, respectivamente. Exame
de congelação da massa ressecada foi realizado rotineiramente
nesta série.

Aspectos
Técnicos
1)- Preparo pré-operatório:
O preparo cirúrgico para LRPL é semelhante ao da cirurgia
aberta, incluindo laxativos leves para higiene colônica e internação
no dia do procedimento, com jejum de 8 horas. Provas cruzadas e reserva
de sangue são realizadas rotineiramente. Cateterismo ureteral para
eventual identificação e/ou proteção dos ureteres
e cateteres peri-durais para analgesia não são por nós
empregados. O procedimento é realizado sob anestesia geral com
intubação oro-traqueal e com passagem de sondas vesical
e nasogástrica, retiradas ao final do procedimento.
2)- Colocação dos trocartes:
Com o paciente em decúbito lateral, um trocarte de 10/11 milímetros
(mm) é inserido na borda lateral do músculo reto abdominal
na altura da cicatriz umbilical. A óptica é introduzida
e utilizada para revisão da cavidade e inserção de
outros 2 trocartes de 10/11 mm, os quais serão os portais de trabalho.
Estes são posicionados em ângulo de 30 graus com o portal
da óptica em média 5 cm acima e abaixo da mesma. Portais
adicionais são inseridos durante a cirurgia dependendo das necessidades
técnicas. Em todos os casos foi utilizada exclusivamente a via
transperitoneal.
3)- Técnica de dissecção:
Após o cólon ser mobilizado medialmente com a incisão
da fáscia de Toldt, os pontos chave da LRPL são definidos:
veia cava, aorta, vasos renais e ureteres. Para procedimentos do lado
direito, ampla liberação do cólon ascendente e duodeno
é imperativa; para o lado esquerdo, o cólon descendente
deverá ser igualmente dissecado e o ligamento espleno-cólico
seccionado para se obter bom acesso ao retroperitônio. A intenção
é realizar a linfadenectomia retroperitoneal modificada, com abordagem
unilateral dos vasos renais (9). O cordão espermático é
o ponto inicial da cirurgia, devendo ser removido completamente a partir
do orifício inguinal interno. Na LRPL direita, o tecido que envolve
a veia cava inferior, os linfonodos inter aorto-cavais, o tecido pré-aórtico
cranial à artéria mesentérica inferior e a área
dos vasos ilíacos comuns são ressecados. O limite superior
da dissecção são os vasos renais. Do lado esquerdo,
a dissecção é similar, incluindo o tecido para-aórtico,
os linfonodos pré-aórticos a partir da artéria mesentérica
inferior e os vasos ilíacos comuns, sendo o limite superior da
dissecção novamente os vasos renais. O campo operatório
não é drenado rotineiramente.
RESULTADOS
LRPL
foi completada nos 5 casos. Em um dos pacientes houve uma laceração
da veia cava inferior que foi controlada com clipagem seqüencial
e sutura vascular laparoscópica com prolene 5-0. Este paciente,
ao final do procedimento, com suturas de pele já realizadas, apresentou
um quadro de hipotensão e foi então realizada uma revisão
videolaparoscópica do retroperitônio que não revelou
alterações significativas, estando íntegra a sutura
da veia cava, tendo o paciente respondido prontamente a hidratação
e drogas vasoativas. O paciente evoluiu bem e recebeu alta 72 horas após
o procedimento. Uma reação vasogênica autonômica
seria a explicação mais plausível, por superficialização
anestésica, por exemplo, ou outro evento cirúrgico menor.
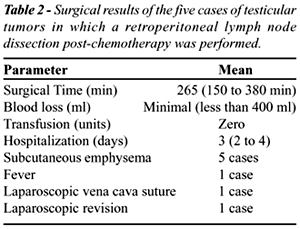
O tempo cirúrgico variou de 150 a
380 minutos (média de 265 minutos). Sangramento intra-operatório
foi pouco volumoso e nenhum paciente recebeu transfusão sangüínea.
O período de hospitalização pós-operatória
variou de 2 a 4 dias (média de 3 dias). A morbidade do pós-operatório
imediato foi mínima, e os pacientes retornaram às suas atividades
habituais entre 2 e 4 semanas. A Table-2 detalha melhor estes dados. O
exame anatomopatológico, tanto de congelação quanto
definitivo em parafina, revelou tecido necrótico em 4 dos pacientes
e teratoma maduro em 1 caso. A ejaculação anterógrada
foi preservada em todos os pacientes. O seguimento varia de 6 a 23 meses,
e até o momento não se observou nenhuma recorrência
clínico-radiológica ou bioquímica da doença.
DISCUSSÃO
Uma
discussão de longa data na literatura urológica diz respeito
à melhor abordagem para tumores testiculares não-seminomatosos
estágio-I. Enquanto alguns advogam seguimento cuidadoso, baseados
na eficácia dos quimioterápicos utilizados no tratamento
desta patologia em particular, outros preferem a linfadenectomia retroperitoneal
com finalidade diagnóstica e terapêutica, enfatizando o fato
de que metástases microscópicas podem coexistir em até
30% dos casos (7). A LRPL parece oferecer uma ótima alternativa
diagnóstica e terapêutica nestes casos (1-3,5,6,8,9).
Outro uso potencial da linfadenectomia retroperitoneal
diz respeito à avaliação da resposta pós-Qt
em pacientes com tumores testiculares de estágio avançado.
Com a disponibilidade de quimioterápicos eficazes de segunda linha,
um diagnóstico adequado pós-Qt inicial pode ser fundamental
para indicação precisa de Qt de resgate ou para comprovação
de boa resposta ao primeiro tratamento em caso de massas residuais. Com
o advento da cirurgia laparoscópica, sua aceitação
crescente e recentes relatos de cirurgias urológicas complexas
realizadas com este método, é imperativa a avaliação
da exiqüibilidade da LRPL pós-Qt nas neoplasias testiculares.
Discussão igualmente polêmica
refere-se às recomendações de linfadenectomia pós-Qt.
Muitos centros não recomendam linfadenectomia retroperitoneal se
a TC pós-Qt for normal, mostrar massa residual com menos de 1.5
cm ou se houver redução de 90% ou mais da massa pós-Qt,
desde que o tumor primário não exiba elementos teratomatosos
(11-13). Por outro lado, outros autores recomendam linfadenectomia retroperitoneal
em todos os pacientes com tumores primários do retroperitônio
com mais de 3 cm, independentemente dos achados tomográficos pós-Qt
(7). Adicionalmente, se pacientes com achados radiológicos negativos
pós-Qt não forem submetidos a linfadenectomia, 8% a 13%
dos casos de teratoma maduro serão “abandonados” no retroperitônio
sem tratamento adequado, uma vez que os mesmos são rádio
e químio-resistentes (14). Nossa prática tem sido indicar
linfadenectomia retroperitoneal pós-QT para todos as massas residuais
acima de 1.5 cm e para todos os tumores primários acima de 5 cm,
independentemente da resposta a Qt, desde que apresentem marcadores tumorais
negativos.
Outra grande controvérsia refere-se
aos limites da linfadenectomia retroperitoneal pós-Qt. Enquanto
alguns autores preconizam linfadenectomia retroperitoneal completa, especialmente
para estágio IIc (15), outros relatam resultados semelhantes com
linfadenectomia retroperitoneal modificada para estágios clínicos
IIb e IIc em casos selecionados, preservando a ejaculação
em 85% dos pacientes (16). Uma abordagem mais elaborada, e por nós
rotineiramente empregada, foi proposta por Herr (17). O autor sugere ressecção
unilateral limitada ou ressecção isolada da massa retroperitoneal
pós-Qt com exame de congelação na sala cirúrgica;
se a mesma demonstrar apenas necrose, a cirurgia poderá ser interrompida
neste ponto com segurança. Esta proposta é, na realidade,
um refinamento dos estudos de Wood et al. que abordaram retrospectivamente
a distribuição de metástases retroperitoneais para
tumores não-seminomatosos pós-Qt (18). Esses autores demonstraram
que empregando-se a dissecção linfonodal modificada numa
população de 113 pacientes pós-Qt e estágio
clínico IIb e IIc, somente 8% teriam tumores fora da área
de ressecção e, destes, todos tinham massas que gerariam
dúvida através de palpação intra-operatória.
Os mesmos pesquisadores concluem que, para pacientes selecionados, a linfadenectomia
retroperitoneal modificada é apropriada neste cenário clínico
pós-Qt. O trabalho também é importante por demonstrar
que a distribuição dos linfonodos pós-Qt em tumores
não-seminomatosos de testículo é semelhante aos sítios
de disseminação primária da neoplasia. Isto implica
que dissecções extensas com ligadura de vasos lombares e
dissecções retrocavais e retroaórticas podem ser
abolidas com segurança na maior parte dos casos. Isto porque as
cadeias linfáticas retrocavais e retroaórticas quase nunca
são os sítios primários das metástases e só
estarão envolvidas em casos realmente avançados com invasão
concomitante de outras cadeias linfonodais mais superficiais. Portanto,
a orientação atual referente à LRPL é que
somente dissecções unilaterais sejam realizadas (9,14).
Nossas indicações têm sido limitadas a tumores retroperitoneais
pós-Qt com tamanho não superior a 5 cm, apresentando-se
como lesão única ou lesões múltiplas unilaterais.
Outra indagação refere-se
a pacientes submetidos a LRPL e com neoplasia ativa na congelação
intra-operatória. Duas abordagens podem ser discutidas com o paciente
antes da cirurgia: a primeira seria a conversão para um procedimento
aberto e realização de linfadenectomia retroperitoneal clássica
bilateral; a segunda seria completar o procedimento por via laparoscópica
como planejado, instituindo Qt adjuvante, uma vez que a mesma é
muito efetiva nestas situações. A conduta é discutível
e passível de críticas.
A exposição adequada e a identificação
dos pontos de referência são fundamentais na LRPL, principalmente
a aorta e a veia cava, vasos renais e ureteres. Para este fim temos sempre
empregado a via transperitoneal, pois a abordagem laparoscópica
retroperitoneal para linfadenectomias extensas nos parece dificultar e
limitar o acesso cirúrgico. A dissecção é
iniciada pela identificação do ducto deferente e cordão
espermático ao nível do anel inguinal interno, que é
ressecado em toda sua extensão. O uso do cautério bipolar
tem se mostrado bastante útil neste contexto, entretanto, a nosso
ver, a utilização do bisturi ultra-sônico é
o que faz realmente diferença, pois, além de ser extremamente
eficaz para corte e coagulação, produz pouco calor e não
opacifica a óptica, permitindo que se poupe tempo valioso, evitando
retiradas freqüentes da mesma para limpeza. Outra vantagem importante
do bisturi ultra-sônico diz respeito à extensão da
queimadura que o mesmo produz; como esta é mínima, o risco
de lesão térmica de vísceras adjacentes é
pequeno durante a dissecção.
Em se tratando de laparoscopia, devemos
ser cuidadosos com a hemostasia. Qualquer sangramento, mesmo que mínimo,
deve ser interrompido e/ou revisado imediatamente. Na literatura, são
citados compostos de fibrina e outros artifícios, como gelfoam,
para parar pequenos sangramentos, ou eventuais sangramentos maiores, inclusive
algumas lacerações de cava (4). Em nossa série inicial
pós-Qt ocorreu um caso de laceração de veia cava
inferior. Esta complicação exige experiência com algumas
manobras laparoscópicas para seu controle adequado. Inicialmente
empregamos gaze laparoscópica para tamponar o orifício,
procedendo-se, então, à clipagem seqüencial cuidadosa
da área da lesão. Quando esta manobra não é
suficiente, temos realizado a sutura da laceração com prolene
5-0, como no caso acima.
Corroborando relato da literatura, a Qt
prévia não tem inviabilizado ou dificultado excessivamente
o procedimento de dissecção laparoscópica (4). Explicações
para este fato podem estar relacionadas à excelente exposição
do retroperitônio após a liberação do cólon,
a magnificação proporcionada pelos aparelhos de vídeo
e câmeras utilizados, à ótima iluminação
das fontes atuais e à pressão exercida pelo gás do
pneumoperitôneo que facilitaria a identificação dos
planos cirúrgicos. Para ilustrar este fato citamos um dos casos
de nossa série em que realizamos LRPL com sucesso em massa residual
pós-Qt de um seminoma testicular direito junto aos vasos ilíacos.
A dificuldade técnica em abordar massas residuais pós-Qt
em tumores seminomatosos é de conhecimento geral. Em relação
à série de Rassweiler et al. (9), que não sugerem
a abordagem laparoscópica para massas residuais pós-Qt,
possivelmente o problema tenha sido relacionado à seleção
de pacientes para cirurgia - dos nove casos operados, sete foram estadiados
clinicamente como IIc (massas com mais de 5 cm). Em nenhum dos sete casos
estágio clínico IIc, o procedimento laparoscópico
se completou, porém, a LRPL foi realizada com sucesso nos dois
pacientes com estágio clínico IIb.
A morbidade da linfadenectomia retroperitoneal
clássica é mínima (5% a 20%), relacionada geralmente
a atelectasias, íleo adinâmico e linfocele, sendo a mortalidade
inferior a 1% (7). Redução adicional destes patamares pós-Qt
empregando a via laparoscópica é um forte atrativo para
a utilização do método, porém cabe enfatizar
que o objetivo final do tratamento é a cura clínica e sobrevida
a longo prazo. Cabe aqui um relato recente da literatura que demonstra
que o controle tumoral dos pacientes submetidos a LRPL pós-QT não
é afetado por esta abordagem (4). Dos 24 pacientes avaliados por
Janetschek et al., com um seguimento médio de 24.4 meses, nenhum
teve evidência de recidiva neoplásica, sendo que os achados
foram de necrose em 71% dos casos, teratoma maduro em 25% e neoplasia
ativa em 4% (4). Porém, devemos frisar que o único paciente
com tumor viável recebeu Qt adjuvante. Os 6 pacientes com achados
histológicos de teratoma da série de Janetschek foram teoricamente
curados pela LRPL, a exemplo de um dos casos por nós relatados,
uma vez que os teratomas retroperitoneais são rádio e químio-resistentes.
No relato de Rassweiler et al., que não sugere LRPL pós-Qt,
nos casos em que foi possível completar o procedimento (2 de 9
casos), o anatomopatológico revelou necrose tumoral e os pacientes
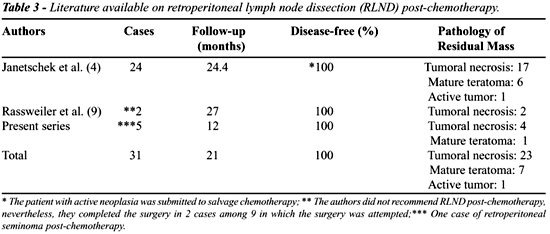
encontravam-se livres da neoplasia (9). A Table-3 contém uma compilação
da literatura demonstrando a sobrevida de pacientes submetidos a LRPL
pós-Qt, incluindo os casos aqui relatados. Apesar da LRPL ter sido
diagnóstica e terapêutica na imensa maioria dos casos descritos
na literatura, esta amostra não representa os dados da literatura
referentes ao procedimento aberto, em que se observam 20% a 33% de neoplasia
ativa para esta condição clínica (7). Tal observação
diminui a validade externa desses estudos, caracterizando-os como ainda
experimentais.
CONCLUSÕES
As neoplasias testiculares avançadas são melhor abordadas com a combinação de Qt e cirurgia. O conceito da Qt primária para neoplasias testiculares estádios IIb e IIc inclui linfadenectomia retroperitoneal para tumores residuais. O esquema quimioterápico usual, empregando o cisplatinum como droga base, proporciona 60% a 70% de resultados satisfatórios sem necessidade de terapia adicional, enquanto aproximadamente um terço dos pacientes deverá ser submetido a linfadenectomia retroperitoneal. Para reduzir a morbidade do procedimento, temos substituído a linfadenectomia clássica aberta pela abordagem laparoscópica em casos selecionados. A LRPL mostrou-se tecnicamente exeqüível pós-Qt para casos com massas únicas e/ou unilaterais múltiplas não superiores a 5 cm. Pacientes com teratoma puderam ser, teoricamente, curados com a ressecção laparoscópica. Apesar de ser um procedimento longo e com algumas complicações potencialmente graves que exigiram habilitação do cirurgião para solucioná-las, apresentou baixa morbidade. A LRPL, embora ainda experimental, representa uma técnica promissora para estadiamento e tratamento de pacientes portadores de neoplasias testiculares, desde que realizada em casos selecionados e em centros com experiência no método.
REFERÊNCIAS
- 1. Giusti G, Beltrami P, Tallarigo C, Bianchi G, Mobilio G: Unilateral laparoscopic retroperitoneal lymphadenectomy for clinical stage I nonseminomatous testicular cancer. J Endourol, 12: 561-566, 1998.
- Janetschek G, Hobisch A, Peschell R, Hittmair A, Bartsch G: Laparoscopic retroperitoneal lymph node dissection for clinical stage I nonseminomatous testicular carcinoma: long-term outcome. J Urol, 163: 1793-1796, 2000.
- Rassweiler JJ, Frede T, Lenz E, Seemann O, Alken P: Long term experience with laparoscopic retroperitoneal lymph node dissection in the management of low stage testis cancer. Eur Urol, 37: 251-260, 2000.
- Janetschek G, Hobisch A, Hittmair A, Holtl L, Peschel R, Bartsch G: Laparoscopic retroperitoneal lymphadenectomy after chemotherapy for stage IIB nonseminomatous testicular carcinoma. J Urol, 161: 477-481, 1999.
- Bianchi G, Beltrami P, Giusti G, Tallarigo G, Mobilio G: Unilateral laparoscopic retroperitoneal lymph node dissection for clinical stage I nonseminomatous germ cell testicular neoplasm. Eur Urol, 33: 190-194, 1998.
- Janetschek G, Hobisch A, Höltl L, Bartsch G: Retroperitoneal lymphadenectomy for clinical stage I nonseminomatous testicular tumor: laparoscopy versus open surgery and impact of learning curve. J Urol, 156: 189, 1996.
- Richie JP: Neoplasm of the testis. In: Walsh PC, Retik AB, Vaughan ED, Wein JA (eds.). Campbell’s Urology.Philadelphia, WB Saunders Company, pp. 2411-2452, 1998.
- Gerber GS, Bissada NK, Hulbert JC: Laparoscopic retroperitoneal lymphadenectomy: multi-institucional analysis. J Urol, 152: 1118-1192, 1994.
- Rassweiler JJ, Seemann O, Henkel TO, Stock C, Frede T, Alken P: Laparoscopic retroperitoneal lymph node dissection for nonseminomatous germ cell tumors: indication and limitations. J Urol, 156: 1108-1111, 1996.
- Cavalli F, Monfardini S, Pizzocaro G: Report on the International Workshop on staging and treatment of testicular cancer. Eur J Cancer, 16: 1367-1370, 1980.
- Stomper PC, Jochelson MS, Garnick MB, Richie JP: Residual abdominal masses after chemotherapy for nonseminomatous testicular cancer: correlation of CT and histology. AJR, 145: 743-746, 1985.
- Donohue JP, Rowland RG, Kopecky K, Steidle CP, Geier G, Ney KG, Einhorn L, Williams S, Loehrer P: Correlation of computerized tomographic changes and histological findings in 80 patients having radical retroperitoneal lymph node dissection after chemotherapy for testis cancer. J Urol, 137: 1176-1180, 1987.
- Fossa, SD, Aass N, Ous S, Hoie J, Stenwing AI, Lien HH, Paus E, Kaalhus O: Histology of tumor residuals following chemotherapy in patients with advanced nonseminomatous testicular cancer. J Urol, 142: 1239-1241, 1989.
- Gelderman WA, Koops HS, Sleijfer DT, Osterhuis JW, Oldhoff J: Treatment of retroperitoneal residual tumor after PVB chemotherapy for nonseminomatous testicular tumors. Cancer, 58: 1418-1421, 1986.
- Freiha FS, Shortliffe LD, Rouse RV, Mark JB, Hannigan JF, Arton D, Spaulding JT, Williams RD, Torti FM: The extent of surgery after chemotherapy for advanced germ cell tumors. J Urol, 132: 915-918, 1984.
- Rabbani F, Goldenberg SL, Gleave ME, Paterson RF, Murray N, Sullivan LD: Retroperitoneal lymphadenectomy for post-chemotherapy residual masses: is a modified dissection and ressection of residual masses sufficient? Brit J Urol, 81: 295-299,1998.
- Herr HW: Does necrosis on frozen-section analysis of a mass after chemotherapy justify a limited retroperitoneal resection in patients with advanced testis cancer? Brit J Urol, 80: 653-656,1997.
- Wood Jr DP, Herr HW, Heller G, Vlamis V, Sogani PC, Motzer RJ, Fair WR, Bosl GJ: Distribution of retroperitoneal metastases after chemotherapy in patients with nonseminomatous germ cell tumors. J Urol, 148: 1812-1816, 1992.
____________________
Received:
May 30, 2001
Accepted after revision: September 25, 2001
_______________________
Correspondence address:
Dr Mirandolino B. Mariano
Rua Costa, 30 / 803
Porto Alegre, RS, 90110-270, Brazil
Fax: + + (55) (51) 231-7247
E-mail: mariano.ez@terra.com.br