EPIDEMIOLOGICAL AND METABOLIC EVALUATION IN RENAL STONE PATIENTS LIVING IN AN SPECIFIC REGION OF BRAZIL
WALDEMAR S. ALMEIDA, NESTOR SCHOR
Division of Nephrology, Paulista School of Medicine, Federal University of São Paulo (UNIFESP), São Paulo, Brazil
ABSTRACT
Objectives:
1)- To evaluate the epidemiological and metabolic factors in renal stone
patients (RSP) in the central region of Brazil; 2)- To study the bone
mass (BW) of RSP with and without hypercalciuria (HCa) [HCa > 4 mg/kg
of BW/24 h] through bone mineral density (BMD).
Material and Methods: RSP (n = 120) have
been studied through a laboratory protocol previously presented. Bone
mineral density was analyzed in 35 patients. Sixteen were hypercalciuric
and nineteen were not.
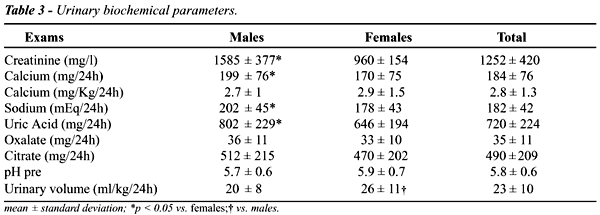
Results: Main metabolic alterations were
hyperuricosuria in 91 (76%); hypocitraturia in 52 (43%); reduced urinary
volume (< 20 ml/kg of BW) in 59 (49%); mild hyperoxaluria in 17 (14%);
renal tubular acidosis in 4 (3%); cistinuria in 2 (2%); idiopathic hypercalciuria
detected in 17 patients (14%). Osteopenia was found in 12 (75%) of the
16 hypercalciuric patients evaluated, especially in 5 (71%) of 7 hypercalciuric
men with average of 29 ± 16 years, and absent in 9 (100%) of 9
normocalciuric men with average of 36 ± 15 years.
Conclusions: 1)- Environmental and nutritional
factors can cause and/or increase the metabolic risk for kidney stone
formation; 2)- It was possible to find out metabolic disturbances in 98%
of RSP, showing a positive relationship between the cost and benefit;
3)- The presence of osteopenia in hypercalciuric young men suggests bone
participation in the pathophysiology and therefore bone evaluation must
be carried through in the presence of this metabolic alteration.
Key words:
kidney calculi; metabolic disease; risk factors; calcium; urolithiasis
Braz J Urol, 27: 432-439, 2001
INTRODUÇÃO
A
nefrolitíase tem aumentado nos países industrializados e
naqueles em desenvolvimento, atingindo de 10% a 15% da população
(1). Nos Estados Unidos, a doença determina de 7 a 10 em cada 1000
admissões hospitalares. A recorrência é de 15% em
1 ano, 50% em 5 anos e chega a 80% em 25 anos, após o primeiro
episódio de cólica nefrética (2).
Na dependência da região estudada
em nosso país, devido à extensão continental, diferenças
climáticas, raciais, sócio-econômico-culturais e de
hábitos alimentares, a morbidade da litíase urinária
tornam a freqüência variável. Desta maneira, estudos
clínicos prospectivos, estudando populações regionais
devem ser realizados para contribuir para o conhecimento das alterações
metabólicas e dos fatores epidemiológicos envolvidos.
Foi estabelecido um ambulatório especializado
em litíase urinária Campo Grande-MS. Esta região
do centro-oeste, que inclui a maior parte do Pantanal Mato-grossense,
tem índice pluviométrico de 1.087,8 milímetros, clima
quente com média anual de 25°C de temperatura, atingindo 39°C
durante o verão e umidade relativa do ar anual em torno de 65%,
sendo que nos meses de inverno esta média chega a níveis
muito reduzidos (< 30%), conforme dados obtidos no Instituto Brasileiro
de Geografia e Estatística (IBGE). A população tem
hábito alimentar rico em proteínas animais, especialmente
carne vermelha, e chá de erva-mate em infusão gelada ou
quente.
MATERIAL E MÉTODOS
Os
pacientes com imagem positiva para cálculo urinário na ultra-sonografia
renal (USR), urografia excretora (UGE) ou passado com episódio(s)
de cólica(s) ou cirurgia do aparelho urinário para retirada
de cálculo, com creatinina plasmática de até 1.3mg%
foram incluídos no estudo.
A investigação foi exclusivamente
ambulatorial, sob dieta e ingestão hídrica habituais na
ausência do uso de medicamentos que alterem a composição
físico-química da urina.
O estudo incluiu 120 pacientes, sendo 56
homens e 64 mulheres com idades de 40 ± 14 e 42 ± 14 anos,
respectivamente.
Na história clínica deu-se
ênfase a antecedentes familiares de litíase e patológicos
como presença de hematúria, infecção urinária,
episódios de cólicas com eliminação espontânea
de cálculo, ou retirados por litotripsia extracorpórea por
Ondas de Choque (LECO)/cirurgia. Outras variáveis como fatores
nutricionais, ambientais, ingestão de líquidos, rendimento
médio mensal e atividade física, também foram examinados.
O rendimento médio mensal das pessoas
de 10 anos ou mais de idade, residentes em área urbana é
dado em salários mínimos segundo a classificação
do IBGE:
a)- mais de 20 salários mínimos; b)- mais de 10 a 20 salários
mínimos; c)- mais de 5 a 10 salários mínimos; d)-
mais de 3 a 5 salários mínimos.
A atividade física diária
foi inferida de acordo com as informações colhidas:
a)- muito leve: sentado, estudando, conversando, em pé até
2 horas; b)- leve: professor, comércio, laboratório, datilógrafo,
caminha pouco; c)- moderada: lides do lar, mecânico, jardinagem,
senta pouco, caminha de 6 a 7 km/dia; d) - pesada: serviço braçal,
dança, atletismo.
Os pacientes inicialmente foram submetidos
a exames laboratoriais: dosagens sangüíneas de creatinina,
cálcio, fósforo, ácido úrico e paratormônio
fração intacta (PTH-i), urocultura com antibiograma e cistina
qualitativa.
Na segunda etapa, sob dieta habitual e com
urocultura negativa, duas coletas de urina de 24 h foram obtidas, com
intervalo mínimo de uma semana, para dosar creatinina, cálcio,
oxalato, citrato, ácido úrico, cistina quantitativa e sódio.
Os frascos para coletar urina para dosagens de cálcio, citrato
e oxalato, continham ácido clorídrico 20 ml/l a 50%. Nos
frascos para coletar urina para dosar o ácido úrico, o conservante
era carbonato de sódio 5 g/l de urina.
Para medir pH urinário, uma amostra
de urina matinal foi colhida sob vaselina, após restrição
de líquidos por 12 h. Se este fosse maior do que 5.5 repetíamos
a medida do pH urinário após sobrecarga oral de cloreto
de amônio (100 mg/Kg de peso). Mantida a incapacidade de acidificação,
o diagnóstico de Acidose Tubular Renal fica estabelecido.
As técnicas laboratoriais utilizadas
foram as convencionais: método enzimático colorimétrico
para ácido úrico, cálcio e cistina; método
de recristalização do ácido amino naftal sulfônico
para o fósforo; método do picrato alcalino, segundo reação
de Jaffé, para a creatinina; reação enzimática
utilizando-se citrato-lyase para o citrato; determinação
quantitativa enzimática usando oxalato oxidase (Sigma Kit) para
o oxalato; através do eletrodo íon seletivo marca AVL Mod.
9180, o sódio; através de pHmetro o pH urinário;
por quimioluminescência (IMMULITE) o PTH-I.
A hiperoxalúria leve (HOxl) foi diagnosticada
quando as dosagens de oxalato na urina eram de 44 - 50 mg/24 h.
Foram solicitados exames de imagem (US,
UGE) para os pacientes que ainda não os tinham realizado ou quando
esses não eram elucidativos.
Em 35 pacientes foi realizada a densitometria
óssea (DMO) da coluna lombar em AP e do 1/3 proximal do fêmur.
Os valores densitométricos utilizados foram os estabelecidos pela
Organização Mundial de Saúde e recomendados pela
Sociedade Brasileira de Densitometria Óssea, considerando-se como
referência o desvio padrão (DP) em relação
à média dos valores do adulto jovem (T score).
Para análise estatística,
aplicaram-se:
1)- teste t de Student para amostras independentes; 2)- teste para comparação
de duas proporções;
3)- teste exato de Fisher. Os resultados foram expressos como média
e desvio padrão (X ± DP). As significâncias estatísticas
foram definidas como p < 0.05.
Foram estudados
120 pacientes litiásicos quanto aos prováveis fatores de
risco, epidemiológicos, metabólicos urinários. As
Tables-1-8 expressam os resultados observados.

DISCUSSÃO
Possivelmente
o somatório: dieta rica em proteína animal, considerada
o principal fator dietético na formação de litíase
renal (3); a maior ingestão de oxalato, no chá de erva-mate
em infusão; características climáticas da região,
que por ser ensolarada é quente no verão e, no inverno de
baixa umidade relativa do ar, sejam os fatores de risco (4), preponderantes
nesta série. Neste estudo foram examinados 120 pacientes litiásicos,
a maioria (93%) da raça branca como noutras séries (5),
provavelmente devido a fatores genéticos, o que explicaria a menor
freqüência da litíase urinária em outras raças,
em especial na raça negra.

Houve maior número de pacientes litiásicos
com atividade física leve e sobrepeso, fatores considerados de
risco para a formação de litíase renal. A nefrolitíase
predominou entre os pacientes das classes B e C, com rendimento médio
mensal superior a 5 salários mínimos, portanto, em pacientes
de maior poder aquisitivo, semelhante a outras séries publicadas
(6-8). Estes dados sugerem aumento no consumo de proteína animal
(9), acarretando anormalidades metabólicas, talvez de maior impacto
que o sedentarismo e a obesidade.
Nesta série, as alterações
metabólicas estiveram presentes em 98% dos casos, sendo que a minoria,
menos de 10%, tinha apenas uma alteração metabólica;
mais de 30%, duas anormalidades e próximo de 60%, três ou
mais alterações. Estes números são expressivos
e confirmam a importância da multiplicidade de fatores na gênese
do cálculo.
É sabido que a HEAcUr têm incidência
bastante variável, dependendo da região estudada, e tem
grande impacto epidemiológico pois esta população
de litiásicos apresenta maior recorrência (10), acrescida
de maior morbidade. Neste estudo foi detectada em 76% dos casos, incidência
elevada quando comparada com a freqüência de 25% verificada
nos EUA (11), entretanto, próxima da incidência relatada
em Israel (75%) (12) e em algumas séries nacionais (13,14), provavelmente
reflexo da grande e variada ingestão de proteína animal,
principal via de produção do ácido úrico.
A elevada ingestão de proteína animal bovina é comum
na população estudada, que tem na pecuária de corte
a grande fonte de renda do Estado. É importante ressaltar que a
hiperuricemia e a hiperuricosúria isoladas foram pouco freqüentes
e que as principais anormalidades metabólicas associadas aqui listadas,
por ordem de freqüência, a hipocitratúria (HCit), hipercalciúria
(HCa) e hiperoxalúria leve (HOxl), também são relacionadas
à dieta. Estes distúrbios metabólicos urinários
múltiplos, somados à diurese reduzida, facilitariam e potencializariam
a saturação da urina, a nucleação, a agregação
e retenção de cristais nos rins, ocasionando alterações
biológicas celulares e moleculares e a formação do
cálculo.
Vale lembrar que em apenas 10% dos pacientes
os cálculos eram radio-transparentes, puros de ácido úrico.
Na grande maioria a nefrolitíase era cálcica, resultante
de cristais de ácido úrico que podem funcionar como núcleo
heterogêneo para promover a cristalização de oxalato
de cálcio ou através de outros mecanismos possíveis
ainda não bem entendidos (10).
A hipocitratúria (HCit) ocorreu isoladamente
em apenas 2% e em 43% dos casos estava associada a outros distúrbios.
Esta freqüência é semelhante a de outros séries
internacionais, que indicam hipocitraturia em 20 a 60% dos pacientes (15,16),
e brasileiras (14,17-19). Estas diferenças poderiam corresponder
a maior e variável ingestão de proteína animal, que
também levaria a outros distúrbios associados nesta série
e descritos em ordem decrescente de freqüência: HEAcUr + HEAcUrm,
HCa e HOxl. Nestes pacientes hipocitratúricos, a presença
de volume urinário reduzido, em 48%, pode estar contribuindo para
a formação de cálculo.

O volume urinário inferior a 20 ml/Kg/24
h em presença de hiperoxalúria e hipocitratúria é
considerado o principal fator indutor da cristalização do
oxalato de cálcio, (20, 21). Além disso, propõe-se
que a lentificação do fluxo urinário favoreça
a retenção de cristais (22). Nesta série foi encontrado
em 49% dos casos, freqüência elevada quando comparada a outras
séries descritas na literatura internacional, que em média
atinge de 13% a 19% dos pacientes com litíase urinária,
bem como nas séries nacionais (14,18,19).
São vários os métodos
utilizados para dosar a oxalúria; nenhum deles é considerado
ideal e, por conseguinte, os valores normais de oxalúria variam
muito na literatura (23). Nesta série, observou-se que a excreção
de oxalato foi de 35 ± 11 mg/24h, numericamente superior aos padrões
de excreção oxalato descritos, que variam entre 27 e 30
mg/24h em pacientes com ingestão de cálcio em torno de 1000
mg/dia (24). Tem sido observado correlação positiva entre
dieta rica em proteína animal e maior oxalúria (25). Além
disso, é importante lembrar que a nossa população
ingere reduzida quantidade de cálcio, o que propiciaria maior absorção
de oxalato e hiperoxalúria leve (44 - 50 mg/24 h) (26), que nesta
série foi encontrada em 14% dos pacientes, número semelhante
quando comparado a outras séries da literatura. No presente estudo,
todos os casos de (HOxl) estavam associados a alguma outra anormalidade
urinária. Aproximadamente 50% da excreção urinária
de oxalato, na maioria dos indivíduos, é dependente do oxalato
dietético. Nos últimos anos tem sido dada maior importância
à oxalúria leve como fator de risco para a litogênese
(27). É sabido que, devido à relação de Ca/Ox
na urina ser de 5 : 1, pequenas alterações nas concentrações
urinárias de oxalato elevam significantemente a saturação
do oxalato de cálcio na urina e o risco de formação
de cálculo (27).

A acidose tubular renal incompleta (ATRi)
foi diagnosticada em apenas 3% dos pacientes litiásicos, freqüência
superior à de outros estudos nacionais (14,17,19). Nos pacientes
com ATRi a hipocitratúria foi significantemente menor em relação
àqueles que normalmente acidificam a urina, propiciando a agregação
de cristais e formação de cálculos urinários.
Talvez o fato mais importante é se ter comprovado que um simples
exame de urina, coletada em jejum sob vaselina após 12 h de restrição
de líquidos e uma segunda coleta após adequada sobrecarga
ácida com cloreto de amônio (28) através de pHmetro,
seja bastante para este diagnóstico.
A cistinúria foi detectada em 2%
dos casos. Na literatura é descrita a sua incidência em 0.05%
na população e em 0.9 a 6.8% em pacientes litiásicos
(15).

A HCa, superior a 4 mg/Kg/24 h para ambos
os sexos, ocorreu em 14%. Incidência aquém de outras citações
(29). Provavelmente, esta diferença de incidência se deva
ao método de dosagem, pois não foi utilizada a espectrofotometria
de absorção atômica, que apresenta maior precisão.
Nos últimos anos tem sido proposto que a hipercalciúria
idiopática seria resultante de reabsorção óssea,
na ausência de hiperparatireoidismo e de hipercalcemia. Em estudo
realizado no nosso meio, concluiu-se que a nossa população
tem reduzida ingestão de cálcio, em torno de 558 ±
329 mg/dia entre as mulheres e 564 ± 220 mg/dia para os homens
(24), o que causaria balanço negativo de cálcio, aumentando
o risco de desmineralização óssea. A dieta rica em
proteína animal, comum entre pacientes litiásicos, causa
acidose metabólica leve e como conseqüência reabsorção
óssea para tamponamento dos íons hidrogênio, além
de redução da reabsorção tubular renal de
cálcio, por efeito direto, ambos contribuindo para a hipercalciúria
(30,31). Mediante estes dados, tem sido postulado um novo critério
diagnóstico para a hipercalciúria, como resultante de uma
doença óssea primária (5,32). Na presente pesquisa
o estudo ósseo foi realizado, através da densitometria (DMO),
em um subgrupo de 35 litiásicos.
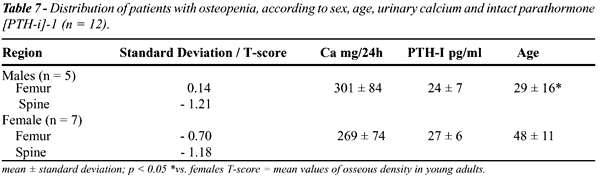
Neste subgrupo a osteopenia esteve presente
em 16% dos pacientes normocalciúricos, todos de sexo feminino,
e em 75% dos pacientes com hipercalciúria que, quando separada
por sexo, atinge 42% e 58% dos homens e mulheres, respectivamente. Esta
freqüência é semelhante à descrita em estudo
recente (33).

Quando os pacientes osteopenicos foram separados
por sexo e idade, detectou-se que os homens jovens hipercalciúricos
apresentavam desmineralização óssea semelhante às
mulheres que tinham mais do que 45 anos de idade. O mesmo não ocorreu
com homens em faixa etária mais elevada e normocalciúricos,
cujas densitometrias ósseas estavam normais em 100%. É necessário
ressaltar que mulheres hipercalciúricas, após a menopausa,
podem ter sua perda óssea intensificada ou acelerada (34). Por
outro lado, a redução da massa óssea em homens é
de fato importante, pois, sabidamente, é reconhecido que homens
apresentam osteopenia só em determinadas situações
patológicas ou iatrogênicas que não estavam até
então relacionadas com a HCa (35). É certo que estudos,
com maior número de casos, prospectivos e randomizados com utilização
de novos marcadores de consumo e produção óssea,
bem como histomorfometria óssea, precisam ser realizados para a
confirmação de que o comprometimento ósseo seja causa
ou conseqüência da hipercalciúria. Espera-se que em
futuro próximo, através de técnicas de biologia celular
e molecular, novas informações permitam que os pesquisadores
adquiram maior conhecimento dos genes responsáveis pela osteogênese,
possibilitando a sua manipulação terapêutica. É
importante lembrar que as dosagens de PTH-I foram normais e comparáveis
nos pacientes com ou sem hipercalciúria (35). Por outro lado, não
se afasta que, apesar de resultados em média normais, possa ocorrer
excesso relativo de PTH-I em pacientes, mesmo dentro da faixa de normalidade.
Foi
possível diagnosticar alterações metabólicas
em 98% dos pacientes estudados, indicando relação muito
positiva entre custo-beneficio.
Medidas dietéticas como aumento da
ingestão hídrica e redução da hiperuricosúria
(através de menor consumo de carne vermelha) poderão contribuir
para a diminuição da formação e recorrência
de cálculo, especialmente de oxalato de cálcio.
A presença de osteopenia em homens
jovens e hipercalciúricos, nesta série, sugere que a hipercalciúria
idiopática seja reabsortiva primária ou secundária
a maior ingestão de proteína animal.
Quando em presença de hipercalciúria
idiopática, sugere-se que seja realizado estudo da densidade mineral
óssea.
REFERÊNCIAS
- Preminger GM, Pak CYC: Nephrolithiasis. In: Jacobson HR, Striker GE, Klahr S (eds.). The Principles and Pratice of Nephrology. St Louis, Sarvier, 149: 1015-103, 1995.
- Wasserstein AG: Nephrolithiasis: acute management and prevention. Dis Mon, 44: 196-213, 1998.
- Curhan GC: Dietary calcium, dietary protein, and kidney stone formation. Miner Electrolyte Metab, 23: 261-264, 1997.
- Soucie JM, Thun MJ, Coates RJ, Mcclellan W, Austin H: Demographic and geographic variability of kidney stones in the United States. Kidney Int, 46: 893-899, 1994.
- Weisinger JR: News insights into the pathogenesis of idiopathic hypercalciuria: The role of bone. Kidney Int, 49: 1507-1518, 1996.
- Goldfarb S: Diet and nephrolithiasis. Annu Rev Med, 45: 235-243, 1994.
- Martini LA, Heilberg IP, Cuppari L, Medeiros FAM, Draibe AS, Ajzen H, Schor N: Dietary habits of calcium stone formers. Braz J Med Biol Res, 26: 805-812, 1993.
- Robertson WG, Peacock M, Heyburn PJ, Hanes FA, Swaminathan R: The Risk of Calcium Stone Formation in Relation to Influence and Dietary Animal Protein. In: Brockis JG, Finlayson B (eds.). Urinary Calculi - International Stone Conference. Littleton, PSG Publishing Co, 1: 3-12, 1981.
- Baumann JM: Stone prevention: why so little progress? Urol Res, 26: 77-81, 1998.
- Bruce Ettinger: Hyperuricosuria and calcim oxalate lithiasis: a critical review and future outlook. Proceedings of the 8th European Symposium on Urolithiasis. Parma, Italy, 51-57, 1999.
- Coe FL: Uric acid and calciun oxalate nephrolithiasis. Kidney Int, 24: 392-403, 1983.
- Atsmon A, Devries A, Frank M: Uric Acid Lithiasis. Amsterdam, Elsevier, pp.1, 1963.
- Pinheiro ME, Schor N: Nefrolitíase por Ácido Úrico. In: Schor N, Heilberg LP (eds.). Calculose Renal. São Paulo, Sarvier, Cap. 7, pp. 53-69, 1995.
- Veronese FV, Giugliani MC, Barros EJG, Mariano M. Multilit - Rio Grande do Sul. In: Schor N, Heilberg IP (eds.). Calculose Renal. São Paulo, Sarvier, Cap. 33, pp. 323-331, 1995.
- Levy FL, Adams-Huet B, Pak CYC: Ambulatory evaluation of nephrolithiasis: an update of a 1980 protocol. Am J Med, 98: 50-59, 1995.
- Pak CYC: Citrate and renal calculi: an update. Miner Electrolyte Metab, 20: 371-377, 1994.
- Heilberg IP, Laranja SMR, Coêlho STSN, Schor N. Multilit - São Paulo. In: Schor N, Heilberg IP (eds.). Calculose Renal. São Paulo, Sarvier, Cap. 33, pp. 336-338,1995.
- Ayusso LL: Desenvolvimento de Serviço de Litíase Renal em Região de Clima Quente. Tese de Mestrado. Escola Paulista de Medicina, Unifesp. São Paulo, 1999.
- Silva JAM, Penido MGMG. Multilit - Minas Gerais. In: Schor N, Heilberg IP (eds.). Calculose Renal. São Paulo, Sarvier, Cap. 33, pp. 307-315, 1995.
- Stapleton FB: Clinical approach to children with urolithiasis. Semin Nephrol, 16: 389-397, 1996.
- Hess B: Diagnostic markers in calcium nephrolithiasis: current and traditional ideas with a new look. Schweiz Med Wochenschr, 125: 2460-2470, 1995.
- Doré B, Dussol B: Lithiase Calcique: Aspects Néphrologiques et Urologiques. In: Encycl Méd Chir. Paris, Elsevier, Néphrologie-Urologie, 18104A40, p.12, 1998.
- Zerwekh JE, Drake E, Gregory J, Griffith D, Hofmann AF, Menon M, Pak CYC: Assay of urinary oxalate: six methodologies compared. Clin Chem, 29:1977-1980, 1983.
- Hess B, Jost C, Zipperle L, Takkinen R, Jaeger P: High-calcium intake abolishes hyperoxaluria and reduces urinary crystallization during a 20-fold normal oxalate load in humans. Nephrol Dial Transplant, 13: 2241-2247, 1998.
- Robertson WG, Heyburn PJ, Peacock M, Hanes FA, Swaminathan R: The effect of high animal protein intake on the risk of calcium-stone formation in the urinary tract. Clin Sci, 57: 285-288, 1979.
- Pak CYC: Kidney stones. Lancet, 351:1797-1801, 1998.
- Willian G. Robertson: Mild hyperoxaluria: a critical review and future outlook. Proceedings of the 8th European Symposium on Urolithiasis - Parma, Italy, pp. 33-42, 1999.
- Lash JP, Arruda JAL: Laboratory evaluation of renal tubular acidosis. Clin Lab Med, 13: 117-129, 1993.
- Heilberg IP, Martini LA, Draibe SA, Ajzen H, Ramos OL, Schor N: Sensitivity to calcium intake in calcium stone forming patients. Nephron, 73: 145-153, 1996.
- Breslau NA, Brinkley L, Hill KD, Pak CYC: Relationship of animal protein-rich diet to kidney stone formation and calcium metabolism. J Clin Endocrinol Metab, 66: 140-146, 1988.
- Goldfarb S: Dietary factors in the pathogenesis and prophylaxis of calcium nephrolithiasis. Kidney Int, 34: 544-555, 1988.
- Weisinger JR, Alonzo E, Bellorín Font E, Blasini AM, Rodriguez MA, Paz Martínez V, Martinis R: Possible role of cytokines on the bone mineral loss in idiopathic hypercalciuria. Kidney Int, 49: 244-250, 1996.
- Trinchieri A, Nespoli R, Ostini F, Rovera F, Zanetti G, Pisani E: A study of dietary calcium and other nutrients in idiopathic renal calcium stones formers with low bone mineral content. J Urol, 3: 654-657, 1998.
- Audran M, Legrand E, Chappard D, Bigorgne JC, Basle MF: Osteoporosis in males. Ann Med Interne, 151: 399-407, 2000.
- Heilberg IP, Martini LA, Szejnfeld VL, Carvalho AB, Draibe AS, Ajzen H, Ramos OL, Schor N: Bone disease in calcium stone forming patients. Clin Nephrol, 42: 175-182, 1994.
____________________
Received: May 30, 2001
Accepted after revision: September 25, 2001
_______________________
Correspondence address:
Dr. Nestor Schor
Rua Botucatu, 740
São Paulo, SP, 04023-900, Brazil
Fax: + + (55) (11) 5573-9652
E-mail: nestor@nefro.epm.br